
Строение и физические свойства воды. Значение, применение и
охрана водных ресурсов.
Цели:
Образовательные:
1) Показать взаимосвязь между строением и физическими свойствами воды;
2) Выяснить, какие свойства воды являются аномальными, и как это влияет на облик планеты.
3) Ознакомить с факторами загрязнения природных вод и путями решения этой проблемы.
Воспитательные:
1) Развивать эстетическое восприятие окружающей природы;
2) Развивать чувство бережного отношения к водным ресурсам.
Развивающие:
1) формировать умение самостоятельно работать с источниками информации;
2) способствовать развитию целостного научного мышления о явлениях, науках, их
взаимосвязи, реализуя межпредметные связи курсов химии, биологии, физики, географии.
Оборудование:
компьютер, мультимедийный проектор, экран, лазерная указка, предметные стёкла, стальные
иголки или металлические скрепки, кристаллизаторы с водой.
Эпиграф (на доске)
Если в столь простом веществе, как вода,
наукой не всё было открыто, то как много ещё
остаётся неясного и точно не исследованного во
всём окружающем нас материальном мире…
Н.Д.Зелинский
Урок начинается со слов Антуана де Сент–Экзюпери (слайд 1)

Вода с одной стороны является самым простым и обычным веществом. В тоже время она может преображаться в самые разнообразные формы в виде дождя, снега, инея, тумана, облака и т. д. И, наверное, поэтому, она была и остаётся источником вдохновения поэтов, художников, композиторов. Поэты и писатели всех времён воспевали в своих произведениях красоту морей и рек, шум водопада, загадочность подводного мира. (слайд 2).

Именно любовь к водной стихии, восхищение его многоликостью помогла создать Айвазовскому Ивану Константиновичу такие шедевры, как «Чёрное море» и «Шторм в ночи». (слайд 3)

А Левитан Исаак Ильич создал свои великие картины «Весна. Большая вода» и «Озеро».

Эти картины, показывающие два противоположных состояния водной глади, как бы показывают состояние души этих великих художников. Какие черты их характера и заветные мечты можно увидеть на этих полотнах? ( По данному вопросу учащимся можно предложить научную работу «Образ (многоликость) воды в творчестве художников, поэтов, писателей»)
Далее учащимся предлагается просмотреть видеофрагменты и сделать вывод.
(слайд 5 )
)
Как предполагаемый вывод можно использовать слова В.И. Вернадского «Нет земного вещества – минерала, горной породы, живого тела, которое её не заключало бы. Всё земное вещество ею проникнуто и охвачено».
Действительно, такие твёрдые вещества,
как гипс и рис в своём составе содержат воду. Её находят в пустынях, которые
называются безводными. Вода содержится в горных породах. Даже в расплавленной
магме она присутствует в значительных количествах и выделяется в виде пара при
извержении вулканов. (слайд 6).
Учитель: Вспомните из курса географии, как распределена вода на территории Земли?
Ученик: Вода покрывает 3/4 (70% земной поверхности)
97 % - солёная вода Мирового океана;
2,2 % - ледники покровные и горные;
0,6 % - пресная вода рек, озёр, подземных горизонтов;
0,2 % - в атмосфере Земли.
(слайд 7)
Учитель: Какую роль играет вода в жизни живых организмов? (Вопрос можно дать заранее группе учащихся по направлениям: 1) для растений; 2) для животных; 3) для человека. (Более подготовленные учащиеся могут создать свои слайды.)
Ученик: Находясь в большом количестве в живых организмах, вода играет огромную роль в их
жизнедеятельности:
• 3500 млн. лет назад в океанах появились первые живые существа. И только благодаря воде жизнь продолжает существовать.
• Живые организмы состоят примерно на ¾ из воды.
•
Большие количества воды потребляют растения. Подсчитано, что для
получения 1 т пшеницы нужно около 1500 т воды, хлопчатника – 10000 т. (слайд 8)

• В человеческом организме 35 л жидкости непрерывно осуществляют «орошение» тела. В этот объём входят: 5л крови, 2 л лимфы, 28 л внутриклеточной и внеклеточной жидкости. Все эти жидкости – водные растворы органических и неорганических веществ.
(слайд 10)

Учитель: Велико значение воды в природе.
• Вода – терморегулятор; (слайд 11)

•

Вода – растворитель, разрушитель и создатель горных пород. (слайд 12)
Учитель: Какое значение имеет большой круговорот воды в обеспечении водой планеты? (слайд 13)

Ученик:
Благодаря круговороту воды на сушу поступает большое количество влаги и тепла. Даже территории, находящиеся далеко от океанов, могут получить необходимое количество воды для питания рек, озёр, подземных вод. Наряду с осадками воздушные массы, приходящие со стороны океана, приносят тепло в зимнее время и прохладу летом. Благодаря круговороту воды суша не становится безжизненной пустыней.
Учитель: Почему воду называют самым аномальным веществом в мире?
Для того чтобы ответить на этот вопрос, выслушаем мнения экспертов, которые работали в разных группах.
Дальше идёт выступление I группы учащихся, которые заранее подготовились по такому заданию:
— Рассмотрите график температур кипения и плавления водородных соединений элементов VI группы главной подгруппы. При какой температуре вода должна кипеть, а при какой – замерзать?
Соответствует ли это действительности? (слайд 14)
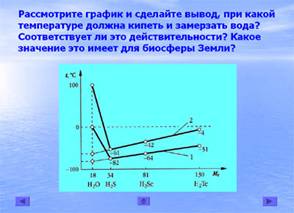
Вывод учащихся:
• При сравнении водородных соединений элементов VI группы видно, что вода должна замерзать при около -100°С, кипеть – около -80°С. На самом деле вода замерзает при 0°С, а кипит при 100°С.
Учитель: Существуют ли на Земле места, где температура ниже -80°С? В каком виде находилась бы вода на планете, если температуры плавления и кипения соответствовали бы графику? К чему бы это привело?
С этим заданием работали учащиеся II группы и они сделали соответствующий вывод:

Задание III группе:
— По какой формуле вычисляется плотность? (![]() =m/V)
=m/V)
— Меняется ли масса воды с изменением температуры? (не меняется)
— Что происходит на холоде с закрытой бутылкой, до краёв наполненной водой? Почему? В какую сторону меняется объём воды при переходе из жидкого состояния в твёрдое? Как при этом меняется плотность?
Вывод:
Задание IV группе учащихся (слайд 16)
Рассмотрите график. Сделайте вывод о значении этого свойства воды для живых существ.
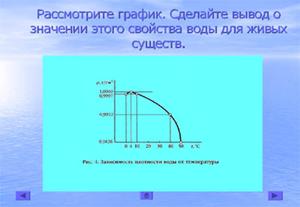
Вывод учащихся:

Задание V группе учащихся: Что такое теплоёмкость? (количество теплоты, необходимое для нагревания 1 кг вещества на 1°С). Чему она равна у воды? [(4,18 Дж/(г·К)]. Какова она у остальных жидкостей? (Работа по справочнику)
Вывод:
глицерин 2,43; этиловый спирт 2,85.
Небольшая лабораторная работа:
Вывод: Вода имеет очень высокое поверхностное натяжение воды – 0,073 Н/м при 20°С. По
прочности на разрыв струя воды не уступает стальной проволоке того же сечения.
Обобщение учителя.
Итак, вернёмся к первоначальному вопросу: «Почему воду называют самым аномальным веществом в мире?»
Учитель: Какова причина всех этих аномалий?
Объяснение учителя:
Молекула воды образуется при взаимодействии двух атомов водорода и одного атома кислорода. Каждый атом водорода имеет один неспаренный s-электрон. В атоме кислорода два неспаренных р-электрона. При перекрывании двух р-электронных облаков атомов кислорода с s-электронными облаками двух атомов водорода образуются две полярные ковалентные связи (слайд 18).

При этом общие электронные пары, образующие химические
связи, смещены к атому кислорода, как к более электроотрицательному элементу. В
структурной формуле это смещение показано знаками
![]() +
и
+
и ![]() -.
р-орбитали взаимно перпендикулярны, и угол между связями должен быть 90°. Но из-за взаимного отталкивания электронных облаков двух
атомов водорода этот угол становится равным 104,5°.
Молекула воды представляет собой диполь. Это значит, что с одной стороны
она имеет положительный заряд (+), а с другой - отрицательный заряд (-).
-.
р-орбитали взаимно перпендикулярны, и угол между связями должен быть 90°. Но из-за взаимного отталкивания электронных облаков двух
атомов водорода этот угол становится равным 104,5°.
Молекула воды представляет собой диполь. Это значит, что с одной стороны
она имеет положительный заряд (+), а с другой - отрицательный заряд (-).
Молекулы воды имеют полярную структуру, чем объясняется их склонность к объединению в более крупные комплексы. Это явление называется ассоциацией молекул. Лед имеет структуру, похожую на структуру воды. В структуре льда есть пустые пространства. Вот почему лед легче, чем вода, и плавает на ее поверхности. (слайд 19)
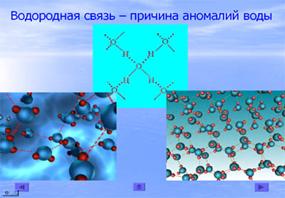
Доказательство ассоциации молекул воды - структура снежинок. Хотя в природе и не существует двух одинаковых снежинок, каждая из них имеет правильную гексагональную форму.
Высокие температуры плавления и кипения также объясняются наличием водородной связи. Прочность четырёх водородных связей соизмерима с прочностью ковалентной связи.
Благодаря полярной структуре молекул вода может растворять другие полярные вещества, например, многие соли, кислоты, щёлочи и т. д. Поэтому вода океанов и морей содержит много растворённых веществ. Даже пресные воды рек и озёр являются растворами многих веществ.
Учитель: Как же получить абсолютно чистую воду?
Вспомним способы разделения смесей. Вода в реке может быть мутной от взвешенных частиц.
Как можно разделить воду от таких примесей?
Ученик: Можно использовать фильтрование. Взвешенные частицы не проходят через фильтровальную бумагу.
Учитель: Но это ещё не чистая вода, она содержит растворённые вещества, которые не остаются на фильтре. Для получения чистой воды её перегоняют нагреванием до кипения с последующим охлаждением пара в приборе, называемом дистиллятором. Такой метод получения чистой воды называется дистилляцией, а сама вода – дистиллированной, которая и обладает всеми вышеуказанными физическими свойствами.
Рассмотрите слайд 20.

Учитель:
Много ли воды на Земле? Сколько воды можно использовать для питья? ( Морская вода не подходит, ледники расположены далеко, подземные воды нужно поднять на поверхность, болотная вода не пригодна для питья. Значит, доступной воды – менее 1 %)
Не только для питья, но и для многих других целей необходима пресная вода. К основным потребителям её относятся: сельское хозяйство (70 %), промышленность, включая энергетику (20 %) и коммунальное хозяйство (15 %). В промышленном производстве наиболее водоёмкими являются химическая, целлюлозно-бумажная и металлургическая промышленность.
Задание:
Принято считать, что житель благоустроенного города расходует в среднем в сутки 250 л воды. Сколько истратит за год семья из четырёх человек?
Потребление человечеством пресной воды неимоверно растёт (слайд 21), особенно с XIX века.
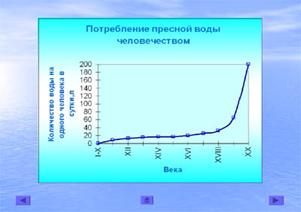
Отсюда вытекает проблема бережного отношения к водным ресурсам.
Основными факторами загрязнения воды являются:
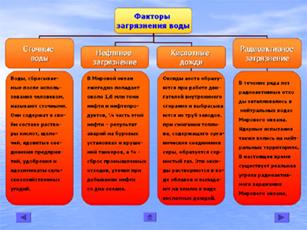
Воды, сбрасываемые после использования человеком, называются сточными. Сточные воды предприятий, содержащие ядовитые вещества, часто сбрасывают в водоёмы без предварительной очистки. В Чувашской Республике сточные воды большинства предприятий проходят очистку на очистных сооружениях примерно по таким стадиям. (видеофрагмент слайда 23)

Основные пути решения проблемы загрязнения водных ресурсов:
· Рациональное использование пресной воды.
· Необходимо строительство очистных сооружений. Использованную воду возвращать в природные водоёмы только после очистки.
· Многократное использование воды на промышленных предприятиях.
· Разработка новых способов очистки вод и переработки промышленных отходов.
· Запрет на проведение ядерных испытаний в водах Мирового океана.
Выводы урока:
Проверку усвоения знаний можно проводить отгадыванием кроссворда.
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
9 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
11 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
12 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
13 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
14 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
15 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
По горизонтали: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
1) Самое аномальное вещество в мире; |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
2) Молекула с противоположно заряженными полюсами; |
|
|
|
|
||||||||||||||||||||||||
|
3) Твёрдое агрегатное состояние воды; |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
4) Объединение частиц в более крупные комплексы; |
|
|
|
|
|
|
||||||||||||||||||||||
|
5) Однородная прозрачная смесь; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
6) Физическая величина, показывающая, какое количество теплоты необходимо сообщить телу, чтобы нагреть его на 1 °С; |
||||||||||||||||||||||||||||
|
7) Водная оболочка Земли; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
8) Переход твёрдого вещества в жидкое; |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
9) Парообразование; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
10) Переход вещества из газообразного состояния в жидкое или твёрдое. |
||||||||||||||||||||||||||||
|
11) Удаление вредных примесей воды; |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
12) Самый распространенный химический элемент Вселенной; |
|
|
||||||||||||||||||||||||||
|
13) Прибор для получения дистиллированной воды. |
|
|
|
|
|
|
||||||||||||||||||||||
|
14) Стадия очистки воды; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
15) Масса единичного объёма вещества. |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
По вертикали: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
1) Причина аномальности воды. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
Подведение итогов.
Список использованной литературы:
• Габриелян О. С. Химия. 8 класс.
• Дергольц В. Ф. Мир воды. – Л.:Недра, 1979.
• Культский Л. А., Даль В. В., Ленчина Л. Г. Вода знакомая и загадочная. – Киев: Радянська школа, 1982.
• Мезенцев В. Энциклопедия чудес. – М.: Знание, 1988.
• Петрянов И. В. Самое необыкновенное вещество в мире. – М.: Педагогика, 1981.
• Электронный учебник по химии. 8 кл. – Просвещение.
• Электронный учебник «Шедевры русской живописи».